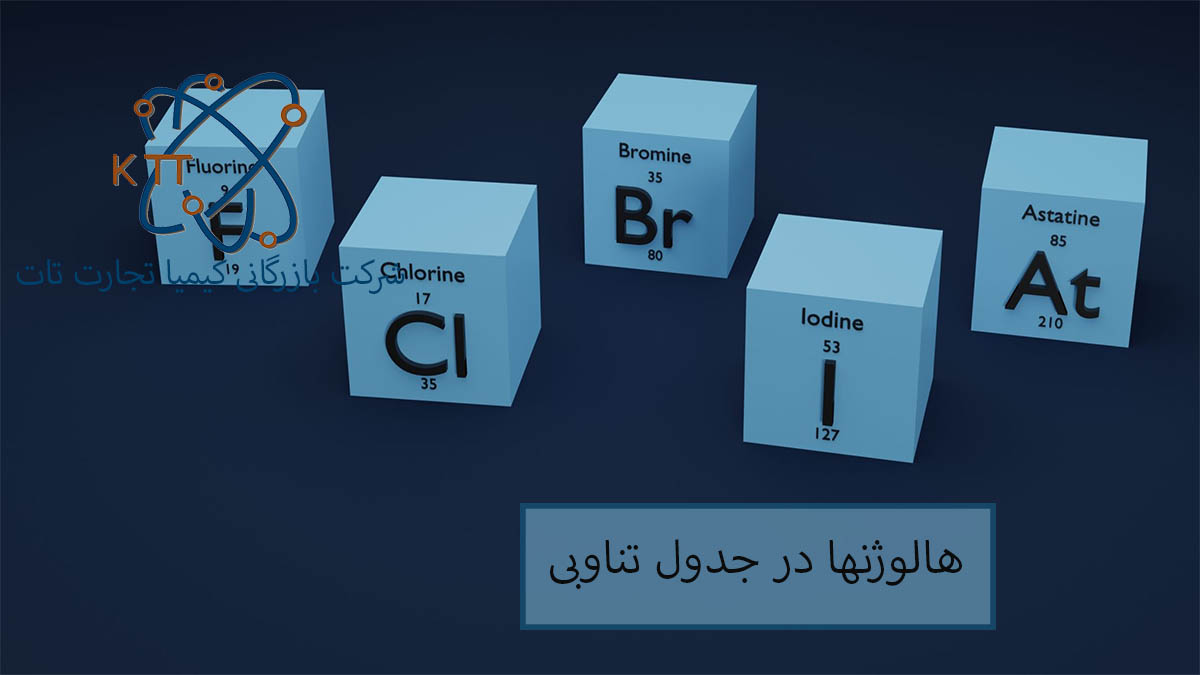
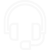اوایل قرن نوزدهم زمان اولیه پیدایش یکی از مهمترین دستاوردهای بشر در علم شیمی می باشد. دیمیتری مندلیف در این سال اصول کلی را برای طبقه بندی عناصر شیمیایی پایه ریزی نمود. این گام مهمی در جهت تولید جدول تناوبی عناصر و دسته بندی دقیق عناصر شیمیایی می باشد. در اصل طبقه بندی عناصر شیمیایی در جدول تناوبی بر اساس افزایش عدد اتمی در ستونها صورت گرفته است. همین امر نیز سبب شد که عناصری که در یک ستون قرار می گیرند عموما دارای خواص شیمیایی مشابهی باشند. در این بین برخی از ستونهای جدول مندلیف دارای خواص مشترکی هستند که تحت یک عنوان کلی نامگذاری می شوند. گازهای نجیب و هالوژنها نمونه بارزی از ستونهای خاص در جدول مندلیف می باشند. در ادامه این متن قصد داریم تا به بررسی عناصر موجود در ستون هالوژنها در جدول مندلیف بپردازیم.
در این مطلب موضوعات زیر را مطالعه خواهید کرد:
بررسی کلی جدول تناوبی عناصر
جدول تناوبی عناصر جدولی می باشد که در آن تمامی عناصری که توسط بشر کشف شده به صورت اصولی طبقه بندی شده اند. به طور معمول جدول مندلیف شامل هفت ردیف افقی می باشد که عناصر در آن براساس عدد اتمی طبقه بندی گردیده اند. در این بین دو ردیف افقی مجزا نیز در جدول تناوبی قرار دارند که مربوط به عناصر گروه لانتانیدها و اکتنیدها می باشد. در تناوب اول این جدول ما تنها شاهد حضور دو عنصر هیدروژن و هلیوم هستیم. هم چنین در دو ردیف بعدی حدود هشت عنصر قرار دارد. در نهایت تعداد عناصر در ردیفهای بعدی جدول تناوبی افزایش می یابد و معمولا تمام عناصر جدول تناوبی به غیر از لانتانیدها و اکتنیدها در این ریفها قرار می گیرند. جدول تناوبی عناصر از 18 گروه تشکیل شده است.
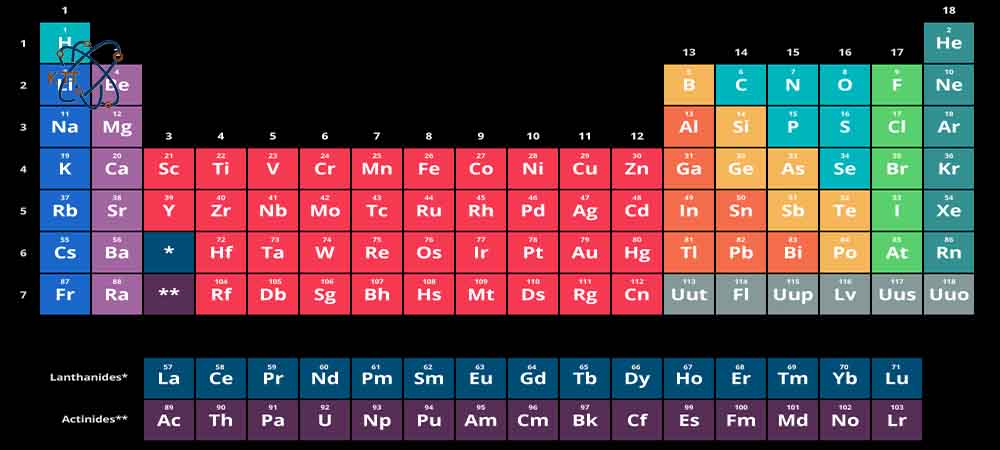
گروه 18 جدول تناوبی به گازهای نجیب اختصاص دارد که شامل عناصری مانند هلیم، نئون، آرگون، کریپتون، زنون، رادون و اوگانسون می باشد. تناوب 1 و 2 جدول تناوبی عناصر نیز به گروه فلزات قلیایی و فلزات قلیایی خاکی تعلق دارد. در نهایت گروه های 13 تا 17 جدول تناوبی عناصر نیز متعلق به گروه بور، کربن، نیتروژن، اکسیژن یا کالکوژنها و در نهایت گروه 17 کلی و 7 اصلی، هالوژنها می باشد.
ستون هالوژنها در جدول تناوبی
گروه 17 جدول تناوبی عناصر به هالوژنها تعلق دارد که شامل عناصری مانند فلوئور، کلر، برم و ید می باشد. ساختار شیمیایی این گروه نیز مانند سایر گروه های جدول تناوبی بر اساس افزایش عدد اتمی از بالای گروه تا پایین آن تقسیم بندی شده است. از دیگر ویژگیهای شیمیایی که در این عناصر مشابه می باشد شامل افزایش جرم مولکولی، نقطه ذوب، نقطه جوش و طول پیوندهای مولکولی در طول جدول هالوژنها است. نیروی بین مولکولی موجود در عناصر گروه هالوژنها از نوع پیوندهای لاندون می باشد. در نهایت هر چقدر به انتهای جدول حرکت می نماییم شاهد افزایش نیروی جاذبه بین مولکولی در عناصر انتهایی این گروه هستیم. همین امر نیز عامل اصلی افزایش نقطه ذوب و جوش در عناصر موجود در گروه هالوژن می باشد.
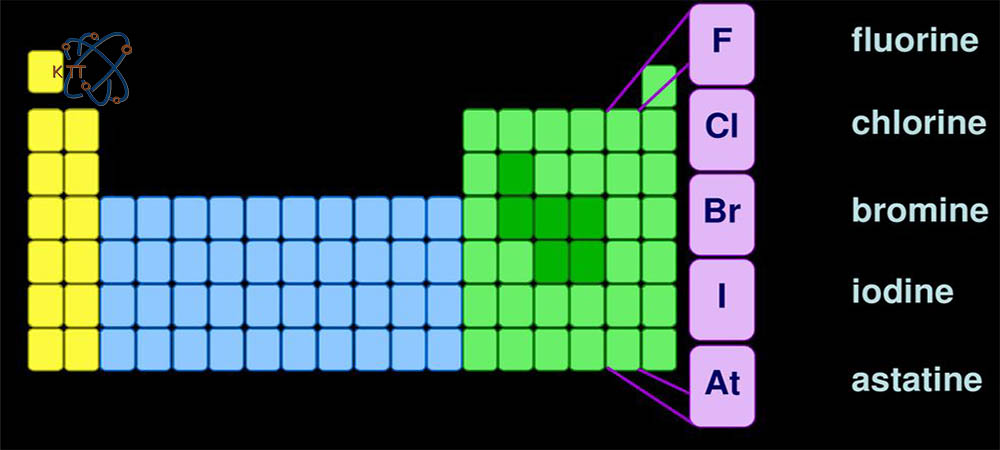
بررسی خواص شیمیایی هالوژنها
هالوژنها شامل عناصر غیر قطبی می باشند که دارای حلالیت بالایی نیز هستند. در نهایت عناصر موجود در گروه هالوژنها به دلیل اینکه تنها یک الکترون کمتر از عناصر موجود در گروه گازهای نجیب دارند همواره تمایل دارند تا در واکنشهایی شرکت نمایند که در آن موفق به جذب یک الکترون شوند. البته باید به این نکته نیز توجه نمود که شدت واکنش پذیری هالوژنها از بالا به پایین جدول کاهش می یابد. در واقع تمامی عناصر موجود در گروه هالوژن به غیر از عنصر فلوئور حاصل واکنش اکسایش هالیدها در مقابل اکسنده هایی مانند دی اکسید منگنز می باشند. فلوئور از عناصری می باشد که دارای میزان بالایی اکسندگی است در نتیجه نمی توان این عنصر را از واکنش اکسیداسیون تولید نمود. در نتیجه فلوئور حاصل فرآیندهای آزمایشگاهی مانند الکترولیز می باشد.
بررسی برخی از واکنشهای هالوژنها
هالوژنها قادر هستند در ترکیبات متعددی حضور پیدا نمایند. هیدروژن هالیدها، متال هالیدها، ترکیبات بین هالوژنی و در نهایت اورگانو هالوژنها تنها بخشی از ترکیبات هالوژنی می باشند که به صورت مختصر به آنها می پردازیم. هیدروژن هالیدها ترکیباتی هستند که از واکنش پذیری گاز هیدروژن با انواع هالوژنها به وجود می آیند. البته افزایش جرم هالوژن سبب کاهش واکنش پذیری در این عناصر می شود. یکی از موارد با اهمیت در واکنش پذیری هالوژنها مربوط به واکنش گاز فلوئور و عنصر هیدروژن می باشد که در هر شرایطی این واکنش به صورت انفجاری می باشد. این در حالی است که برای واکنش سایر عناصر گروه هالوژنها با عنصر هیدروژن شما باید برخی از شرایط مانند شعله، نور و گرما را مهیا نمایید. هیدروکلریک اسید و یا هیدروبرمید اسید برخی از عناصری می باشند که طی واکنش کلر و برم با هیدروژن حاصل می شوند.

دسته دیگر گروه متال هالیدها می باشند. تمامی عناصر موجود در گروه 17 جدول مندلیف قادر هستند تا با سدیم وارد واکنش شیمیایی شوند. در نهایت این واکنش منجر به تشکیل عناصری مانند سدیم فلوراید، سدیم کلرید، سدیم برمید و سدیم یدید می شود. البته عناصر مربوط به گروه هالوژن می توانند با آهن نیز وارد واکنش شوند و سبب ایجاد عناصری مانند آهن کلرید، آهن فلودید و یا آهن برمید شوند. البته باید به این نکته نیز اشاره نمود که غالبا آهن با برمید واکنش پذیری کمتری دارد و این امر در رابطه با عنصر ید نیز صدق می نماید. همچنین در بسیاری از فرآیندها از واکنش هالوژن دار نمودن آلکانها استفاده می نمایند که در نهایت این فرایند منجر به تولید آلکیل هالیدها می شود. باید به این نکته توجه کرد که آلکید هالیدها از آلکانهایی تشکیل می شوند که یک یا چند هیدروژن موجود در ساختار آنها با هالوژن عوض شده است.
کاربردهای هالوژنها
همانگونه که گفتیم واکنش آلکیل هالیدها از مهمترین واکنشهایی می باشد که در گروه هالوژنها شاهد آن می باشیم. در واقع مواد حاصل از این واکنش مهم در تولید انواع محصولات مانند حشره کشها، باکتری کشها، حلالها و در نهایت بیهوش کننده ها استفاده می شود. همچنین می توان به این نکته نیز اشاره نمود که از عناصر گروه 17 جدول مندلیف در تولید لامپها و ترکیبات دارویی نیز استفاده می شود. از دیگر کاربرد هالوژنها می توان به تولید ترکیبات ضد عفونی کننده مانند انواع سفیدکننده ها اشاره نمود. همچنین عموما هالوژنهایی مانند فلوئور، کلر، ید و برم در ساختار بیولوژیکی موجودات زنده تاثیرات بسزایی می گذارند. در نتیجه وجود این عناصر در ساختار بدن موجودات زنده امری کاملا الزامی می باشد.
سوالات متداول هالوژنها در جدول تناوبی
1- آیا هالوژنها دارای ایزوتوپهای متفاوتی هستند؟
در پاسخ به این پرسش می توان اینگونه بیان نمود که هالوژنهایی مانند فلوئور، کلر دارای بیش از دو ایزوتوپ در طبیعت می باشند. این در حالی است که عنصر برم دارای دو ایزوتوپ پایدار و ید دارای یک ایزوتوپ پایدار می باشد.
2- آیا عناصر گروه 17 جدول تناوبی عناصری سمی هستند؟
بله هالوژنها در کل موادی سمی می باشند که سمیت آنها با افزایش جرم اتمی عنصر کاهش می یابد. یکی از سمی ترین عناصری که در طبیعت کشف شده است گاز فلوئور می باشد که استنشاق آن می تواند سبب مرگ شود.
3- مفهوم ترکیبات بین هالوژنی به چه معنا است؟
ترکیبات بین هالوژنی به صورت فرمول شیمیایی XYN معرفی می شود. در این فرمول به جای X و Y هالوژن در معادله قرار می گیرد و N نیز به مفهوم اعداد صحیح 1، 3، 5 و 7 می باشد.
4- مفهوم کلی ارگانو هالوژنها به چه معنایی است؟
برخی از هالوژنها در ترکیبات آلی سنتز شده نقش مهمی را ایفا می نمایند. مانند گاز کلر که در دریاها و اقیانوسها میزان بالایی دارد و در عملکرد مناسب مغز انسان موثر می باشد.
5- آیا افزایش عدد اتمی باعث افزایش واکنش پذیری هالوژنها می شود؟
در پاسخ به این سوال می توان اینگونه بیان نمود که در واقع افزایش میزان عدد اتمی در هالوژنها سبب کاهش میزان واکنش پذیری این عناصر مهم می شود. همچنین در بین تمامی هالوژنها فلوئور بیشترین میزان واکنش پذیری را دارد.