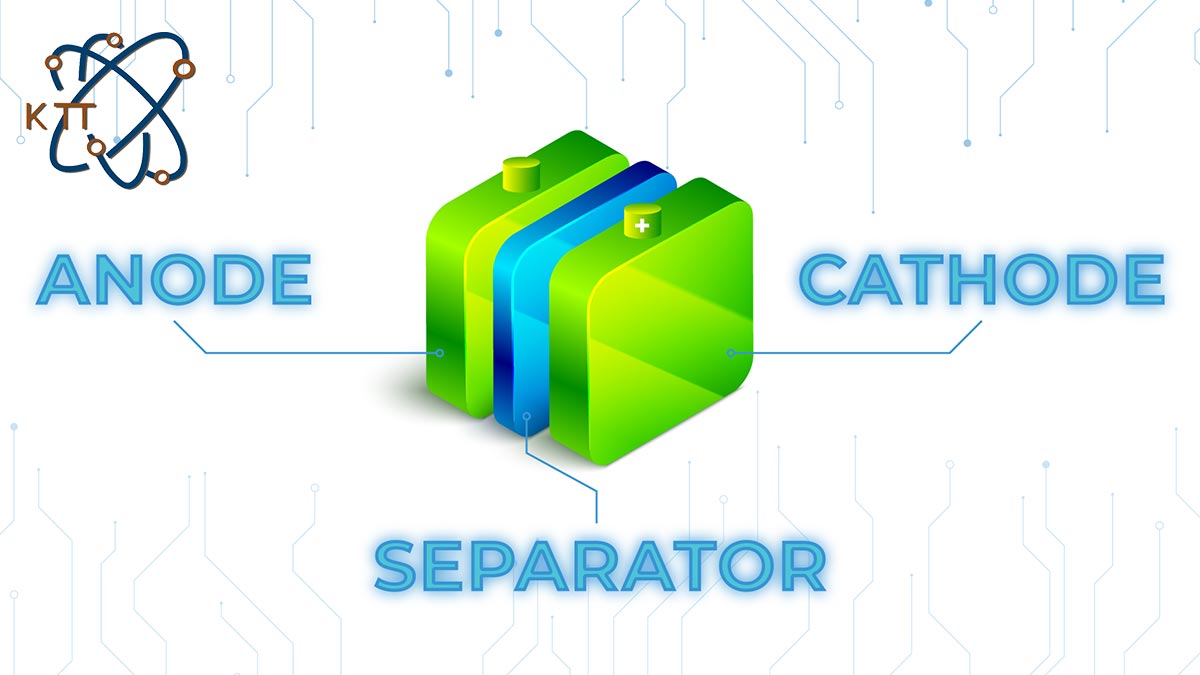
پیش از اینکه بخواهیم با مفهوم کاتد و آند آشنا شویم، لازم است تا با مفهوم دیگری به نام الکترود آشنا شویم. تعریف الکترود را می توان این گونه بیان کرد که الکترود ماده ای است که به هدایت الکتریسیته کمک می کند. در این ماده، جریان الکتریکی مانند یک سلول الکترولیتی به محیط غیر فلزی وارد یا خارج می شود. به زبان ساده تر، الکترود رسانایی است که به برقراری تماس الکتریکی با بخش غیر فلزی مدار کمک می کند. الکترودها از دو قسمت اصلی تشکیل می شوند که کاتد و آند نام دارند. در این مطلب قصد داریم تا به بررسی کاتد و آند بپردازیم و نکاتی که لازم است در رابطه با این موضوع بدانید را به صورت کامل شرح دهیم.
در این مطلب موضوعات زیر را مطالعه خواهید کرد:
کاتد و آند را بشناسیم
بعد از آشنا شدن با الکترود، می خواهیم بدانیم که به صورت کلی کاتد و آند چیست و دقیقا به چه معناست؟ کاتد الکترودی است که جریان از یک دستگاه الکتریکی پلاریزه خارج می شود. آند نیز الکترودی است که جریان از آن وارد یک دستگاه الکتریکی پلاریزه می شود. اصلاح کاتد و آند برای اولین بار در سال 1834 توسط ویلیام ویول به کار برده شد. ریشه کلمه کاتد از واژه یونانی کاتودوس که به معنای نزول است، می باشد. ویلیام برای نامگذاری آن با فارادی مشورت کرده بود.
کاتد چیست؟
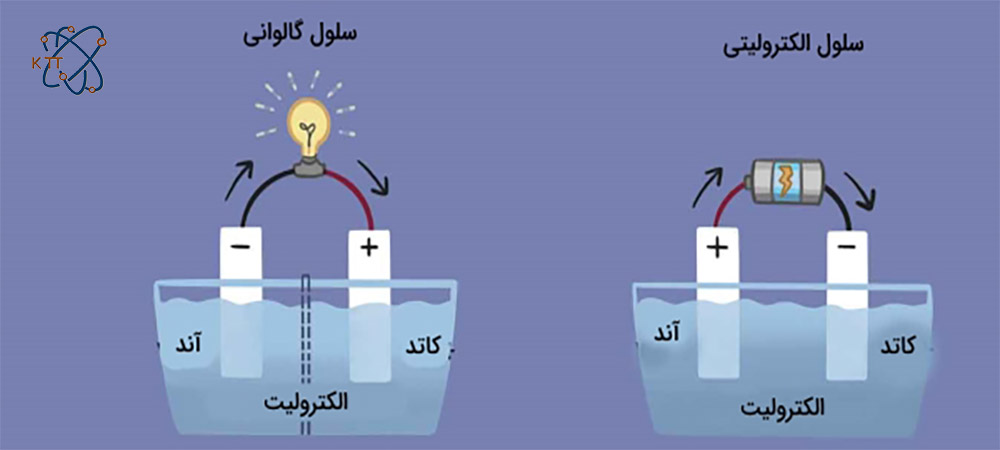
وقتی در رابطه با کاتد در شیمی صحبت می شود، منظور الکترودی است که در آن فرآیند کاهش رخ می دهد. این مفهوم در رابطه با سلول الکتروشیمیایی نیز صدق می کند. در یک سلول الکتروشیمیایی، کاتد منفی است؛ چرا که انرژی الکتریکی که به سلول وارد می شود منجر به تجزیه ترکیبات شیمیایی می شود. با این وجود کاتد می تواند مثبت هم باشد. بعنوان مثال در سلول گالوانیکی که در آن یک واکنش شیمیایی، منجر به تولید انرژی الکتریکی می شود، کاتد مثبت است. کاتد به دو صورت وجود دارد. کاتد گرم و کاتد سرد از جمله انواع کاتد هستند. کاتدی که در حضور فیلامنت گرم می شود تا الکترونها را ساطع کند، به عنوان کاتد گرم شناخته می شود. در حالی که کاتد سرد توسط هیچ فیلامنتی گرم نمی شود.
آند چیست؟
در مفهوم پایه ای، آند در الکتروشیمی به نقطه ای گویند که در آنجا واکنش اکسیداسیون رخ می دهد. به صورت کلی، در آند، یونها یا آنیونهای منفی به دلیل پتانسیل الکتریکی آن، تمایل به واکنش دادن دارند و الکترون به اشتراک می گذارند. این الکترونها به سمت بالا حرکت کرده و وارد مدار محرک می شوند. در یک سلول گالوانیکی، آند طبیعت منفی دارد و الکترونها بیشتر به سمت قسمت خارجی مدار حرکت می کنند. همچنین آند می تواند یک صفحه یا یک سیمی باشد که دارای بار مثبت اضافی است.
الکترولیت چیست؟
الکترولیت محیطی است که در آن انتقال یون بین کاتد و آند در یک سلول انجام می شود. الکترولیتها اغلب مایعاتی مانند آب یا سایر حلالها هستند که با نمکهای محلول و اسیدهای مختلف ترکیب شده اند که برای هدایت یونی لازم هستند. البته باید توجه داشته باشید که الکترولیت لزوما مایع نیست بلکه می تواند جامد هم باشد. به عنوان مثال در بسیاری از باتریها از الکترولیتهای جامد استفاده می شود که نقش رسانایی یونی را در دمای اتاق بر عهده دارند.

تفاوت بین آند و کاتد
آند یک الکترود است که الکتریسیته به آن وارد می شود در حالی که کاتد یک الکترود است که الکتریسیته از آن خارج می شود. آند معمولا قسمت مثبت الکترود است در حالی که کاتد معمولا قسمت منفی الکترود است. معمولا آند به عنوان دهنده الکترون عمل می کند در حالی که کاتد نقش گیرنده الکترون را دارد. در یک سلول الکتروشیمیایی، واکنش اکسیداسیون در قسمت آند و واکنش کاهش در سلول الکتروشیمیایی در قسمت کاتد رخ می دهد. در سلول گالوانیکی، آند می تواند تبدیل به کاتد شود و همچنین کاتد نیز می تواند نقش آند را ایفا کند.
چه موادی می توانند بعنوان کاتد و آند بکار روند؟
مواد مختلفی می توانند به عنوان آند استفاده شوند که موادی مانند روی، لیتیوم، گرافیت یا پلاتین می توانند نقش آند را ایفا کند. ماده ای برای آند مناسب است که هدایت الکتریکی مناسب و قدرت بالایی برای خروج الکتریسیته داشته باشد. کاتد می تواند هر ماده ای باشد تا زمانی که بتواند عامل اکسید کننده را در تماس با الکترولیت داشته باشد. اکسیدهای فلزی می توانند ماده ای بسیار خوب برای استفاده به عنوان کاتد باشند؛ چرا که آنها مقدار قابل توجهی ولتاژ قابل استفاده دارند. موادی مانند اکسید مس، اکسید لیتیوم یا اکسید گرافیت از جمله این مواد هستند.
دلیل اهمیت کاتد و آند در باتری در چیست؟
توجه داشته باشید که مفهوم کاتد و آند یک مفهوم قراردادی است که جهت جریان را نشان می دهد. بنابراین بعنوان مثال کاتد، الکترودی است که الکترون می گیرد و یا جریان الکتریکی از آن خارج می شود. بنابراین در یک باتری که در حال مصرف شارژ است، قطب مثبت کاتد خواهد بود در حالی که در یک باتری در حال شارژ، قطب منفی کاتد خواهد بود. اینکه بدانید تفاوت کاتد و آند در یک باتری چیست، بسیار مهم است. چرا که بدین ترتیب می توانید درک کنید که باتریها چگونه کار می کنند. به عنوان مثال در مواقعی که می خواهید ماشین خود را باتری به باتری کنید، می دانید گیره های اتصال را باید روی یک قطب منفی و دیگری را روی قطب مثبت بگذارید.

سایر موارد کاربرد کاتد و آند
کاتد و آند در جاهای دیگری به جز باتری نیز کاربرد دارند. به عنوان مثال در کشتیها از آندهای قربانی استفاده می شوند که به عنوان محافظ برای کاتد عمل می کنند. این موضوع باعث می شود تا ماده ای که به عنوان کاتد به کار برده می شود در مقابل با خوردگی عملکرد بهتری داشته باشد. آندها در لوازم خانگی نیز به کار برده می شوند. آب گرم کنها دارای میله های آند قربانی هستند که باعث افزایش عمر مفید آب گرم کن می شود. این میله آند، مواد معدنی موجود در آب را جذب می کند و به جای خود مخزن خورده می شود، به همین دلیل نام آند قربانی را روی آن قرار داده اند.
آندها همچنین می توانند به محافظت از مخازن سیال و لوله ها در برابر خوردگی کمک کنند. به صورت کلی نقش آندها معمولا حفاظت از کاتد (ماده ای است که سازندگان می خواهند از آن حفاظت کنند) است. کاتد نیز مانند آند کاربردهای زیادی دارد و در جاهای مختلفی از آن استفاده می شود. از کاتدهای داغ در لوله های خلا در فرستنده های رادیویی استفاده می شود. همچنین برای تولید پرتوهای الکترونی در تلویزیونها و نمایشگرهای کامپیوترهای قدیمی از پرتو کاتدی استفاده می شود. در میکروسکوپهای الکترونی، ژنراتورهای اشعه ایکس و لوله های فلوئورسنت نیز از کاتد استفاده می شود.
سوالات متداول همه چیز درباره کاتد و آند
1- بار کاتد و آند در یک سلول گالوانیکی چیست؟
آند در سلول گالوانیکی دارای بار منفی است در حالی که کاتد دارای بار مثبت است. آند منشا الکترون است و جایی که الکترون در آن جریان دارد، کاتد است.
2- آیا واکنش کاهش همیشه در کاتد رخ می دهد؟
بله واکنش کاهش همیشه در کاتد رخ می دهد و واکنش اکسیداسیون نیز همیشه در سمت آند رخ می دهد. واکنش کاهش در اثر اضافه شدن الکترون رخ می دهد.
3- آیا الکترونها از کاتد به آند می روند؟
به صورت کلی جهت جریان از آند به کاتد است و به همین دلیل است که الکترون از کاتد به آند منتقل می شود. بنابراین در یک سلول الکترولیتی، کاهش در کاتد و اکسیداسیون در آند رخ می دهد.
4- چرا از روی به عنوان آند استفاده می شود؟
روی یکی از بهترین مواد برای استفاده به عنوان آند قربانی است. روی یک ماده فلزی بسیار فعال است که می تواند به عنوان آند قربانی استفاده شود. ازآند روی بیشتر در کاربردهای دریایی مانند بدنه قایقها، مخازن و اسکله ها استفاده می شود.
5- آیا آلومینیوم آند بهتری از روی است؟
آلومینیوم به طرز قابل توجهی از روی سبک تر است. آند آلومینیوم برای حمل و جا به جایی سبک تر و راحت تر است. همچنین ظرفیت الکتروشیمیایی آلومینیوم نسبت به روی بیشتر است. این موضوع بدین معنی است که با مقدار کم تری آلومینیوم می توانید همان مقدار محافظتی که از روی حاصل می شود را به دست آورید.